El mundo que nos rodea, desde el aire que respiramos hasta los alimentos que comemos y la tecnología que usamos, está construido a partir de combinaciones químicas.
Estas combinaciones dan lugar a sustancias con propiedades únicas y fascinantes, conocidas como compuestos químicos.
Comprender qué son y cómo se forman es dar el primer paso para desentrañar los secretos de la materia.
Un compuesto no es una simple mezcla; es una unión íntima y estable entre átomos de diferentes elementos, una transformación que crea algo completamente nuevo.
A diferencia de una mezcla, como el agua salada, donde el agua y la sal conservan sus identidades y pueden separarse por medios físicos como la evaporación, los componentes de un compuesto químico están ligados por fuerzas poderosas.
Pensemos en el agua (H₂O): está formada por hidrógeno, un gas altamente inflamable, y oxígeno, un gas que aviva las llamas.
Sin embargo, al combinarse, forman un líquido estable y esencial para la vida que, lejos de ser inflamable, se usa para apagar el fuego.
Esta transformación radical de propiedades es la característica distintiva de un compuesto. A lo largo de este artículo, exploraremos diversos ejemplos de compuestos para ilustrar su diversidad y su importancia en nuestra vida diaria.
El estudio de los compuestos químicos es fundamental en campos tan variados como la medicina, la ingeniería, la biología y la geología.
Desde el desarrollo de nuevos fármacos, como el ácido acetilsalicílico (C₉H₈O₄), hasta la creación de materiales innovadores como los polímeros, todo se basa en la capacidad de los elementos para unirse y formar estructuras complejas.
A continuación, nos adentraremos en su definición precisa, sus principales tipos y las formas en que los científicos los representan, utilizando fórmulas que son el lenguaje universal de la química.
¿Qué es exactamente un compuesto químico?
Un compuesto químico es una sustancia pura formada por la unión de dos o más elementos químicos diferentes, en proporciones fijas y definidas.
Esta proporción fija es una ley fundamental, conocida como la Ley de las Proporciones Definidas, y significa que la composición de un compuesto es siempre la misma, sin importar su origen.
Por ejemplo, una molécula de agua siempre tendrá dos átomos de hidrógeno por cada átomo de oxígeno (H₂O), ya sea que provenga de un río, de un glaciar o se sintetice en un laboratorio.
Es crucial no confundir un compuesto con una molécula de un solo elemento. El dioxígeno (O₂), que forma la mayor parte del oxígeno que respiramos, o el ozono (O₃), que nos protege de la radiación ultravioleta, son moléculas, pero no compuestos, porque están formadas por átomos de un único elemento: el oxígeno. Para que exista un compuesto, debe haber una diversidad elemental.
La unión entre estos átomos diferentes se produce a través de enlaces químicos, que son fuerzas de atracción que mantienen a los átomos juntos y que solo pueden romperse mediante una reacción química, como la electrólisis que separa el agua en hidrógeno y oxígeno.
La formación de un compuesto implica una reorganización de los electrones de los átomos participantes, lo que resulta en una sustancia con una identidad y un conjunto de propiedades fisicoquímicas completamente nuevas.
El sodio (Na), un metal blando y altamente reactivo que explota en contacto con el agua, y el cloro (Cl), un gas verdoso y tóxico, se combinan para formar cloruro de sodio (NaCl), la sal de mesa común, una sustancia cristalina, estable y esencial para la vida.
Este cambio drástico es la prueba irrefutable de que se ha formado una nueva entidad química, un compuesto.
La Clasificación Fundamental: Compuestos Orgánicos e Inorgánicos
Una de las formas más amplias y tradicionales de clasificar los compuestos químicos es según su origen y composición, dividiéndolos en dos grandes reinos: los orgánicos y los inorgánicos.
Esta distinción, aunque con algunas excepciones y zonas grises, sigue siendo increíblemente útil para organizar el vasto universo de la química.
Los compuestos orgánicos son aquellos cuya estructura principal se basa en cadenas de átomos de carbono, a menudo combinados con hidrógeno, oxígeno, nitrógeno y otros elementos.
Originalmente, se pensaba que los compuestos orgánicos solo podían ser producidos por seres vivos, de ahí su nombre.
Hoy sabemos que pueden sintetizarse en el laboratorio, pero la definición se mantiene centrada en el carbono. Este elemento tiene la asombrosa capacidad de formar enlaces estables consigo mismo y con otros elementos, creando cadenas y anillos de enorme complejidad y variedad.
Esto da lugar a las moléculas de la vida, como la glucosa (C₆H₁₂O₆), el combustible de nuestras células; los aminoácidos, que forman las proteínas; o el etanol (C₂H₅OH), presente en las bebidas alcohólicas.
El metano (CH₄), el principal componente del gas natural, es un compuesto quimico ejemplo de la estructura orgánica más simple.
Por otro lado, los compuestos inorgánicos son todos aquellos que no están basados principalmente en el carbono (con algunas excepciones como los carbonatos y los cianuros, que tradicionalmente se estudian en química inorgánica).
Este grupo abarca una diversidad inmensa de sustancias, desde las más simples hasta las más complejas.
Aquí encontramos el agua (H₂O), el amoníaco (NH₃), los ácidos como el ácido sulfúrico (H₂SO₄), las bases como el hidróxido de sodio (NaOH) y la mayoría de las sales y minerales que componen la corteza terrestre, como el óxido de hierro (III) (Fe₂O₃), conocido comúnmente como herrumbre.
El Vínculo que los Une: Compuestos Iónicos

Adentrándonos en la naturaleza de los enlaces, encontramos una clasificación basada en cómo se unen los átomos.
Los compuestos iónicos se forman por la atracción electrostática entre iones de carga opuesta. Este proceso generalmente ocurre entre un elemento metálico, que tiende a perder electrones para formar un ion positivo (catión), y un elemento no metálico, que tiende a ganar esos electrones para formar un ion negativo (anión).
La transferencia de electrones es el evento clave en la formación de este tipo de enlace.
El cloruro de sodio (NaCl) es el arquetipo de un compuesto iónico. El átomo de sodio (Na) cede su único electrón de la capa más externa al átomo de cloro (Cl), que necesita un electrón para completar su propia capa.
Como resultado, el sodio se convierte en el catión Na⁺ y el cloro en el anión Cl⁻.
Estas partículas cargadas se atraen mutuamente con una fuerza intensa, formando una red cristalina tridimensional muy ordenada y estable.
Esta estructura explica por qué los compuestos iónicos suelen ser sólidos a temperatura ambiente, con altos puntos de fusión y ebullición.
Un gran ejemplo de compuesto iónico es el sulfato de cobre (II) (CuSO₄), un sólido cristalino de un característico color azul.
En disolución acuosa o cuando se funden, los compuestos iónicos tienen una propiedad muy interesante: conducen la electricidad.
Esto se debe a que, en estado líquido o disueltos, los iones (Na⁺ y Cl⁻, por ejemplo) quedan libres para moverse y transportar carga eléctrica.
Otros ejemplos comunes de compuestos iónicos incluyen el yoduro de potasio (KI), utilizado como suplemento nutricional, el nitrato de plata (AgNO₃), con propiedades antisépticas, y el carbonato de calcio (CaCO₃), el principal componente de las rocas calizas, el mármol y las conchas de los moluscos.
Compartiendo para Existir: Compuestos Moleculares o Covalentes
A diferencia de la transferencia de electrones que caracteriza a los compuestos iónicos, los compuestos moleculares, también llamados covalentes, se forman cuando los átomos, generalmente de elementos no metálicos, comparten pares de electrones para alcanzar una configuración electrónica más estable.
Estas unidades discretas y eléctricamente neutras que se forman se denominan moléculas. El enlace covalente es como un pacto de cooperación entre átomos, donde ambos contribuyen y se benefician de los electrones compartidos.
El agua (H₂O) es el ejemplo por excelencia de un compuesto molecular. Cada átomo de hidrógeno comparte su único electrón con el átomo de oxígeno, y a su vez, el oxígeno comparte un electrón con cada hidrógeno. De esta manera, el oxígeno completa su capa externa con ocho electrones y cada hidrógeno con dos, alcanzando la estabilidad.
Otros ejemplos omnipresentes son el dióxido de carbono (CO₂), que exhalamos y que las plantas utilizan para la fotosíntesis, y el metano (CH₄), un potente gas de efecto invernadero.
Las propiedades de los compuestos moleculares suelen ser muy diferentes a las de los iónicos.
Dado que las fuerzas entre las moléculas individuales (fuerzas intermoleculares) son generalmente más débiles que la atracción entre iones en una red cristalina, muchos compuestos covalentes son gases o líquidos a temperatura ambiente, o sólidos con bajos puntos de fusión.
El azúcar de mesa, o sacarosa (C₁₂H₂₂O₁₁), y el alcohol etílico (C₂H₅OH) son ejemplos de compuestos moleculares que, a diferencia de las sales, no conducen la electricidad cuando se disuelven en agua porque no se disocian en iones.
Estructuras Sofisticadas: Complejos o Compuestos de Coordinación

Existe una tercera categoría fascinante de compuestos que combina características de los enlaces iónicos y covalentes: los complejos o compuestos de coordinación.
Estas estructuras se caracterizan por tener un átomo o ion metálico central (generalmente un metal de transición) unido a un grupo de moléculas o iones neutros que lo rodean, llamados ligandos.
El enlace entre el metal central y los ligandos es un tipo especial de enlace covalente conocido como enlace covalente coordinado o dativo, en el cual uno de los átomos (el ligando) aporta los dos electrones que se comparten.
Estos compuestos son cruciales en muchos procesos biológicos e industriales. Un ejemplo biológico de vital importancia es la hemoglobina, la proteína que transporta el oxígeno en nuestra sangre.
En su centro contiene un ion de hierro (Fe²⁺) coordinado con una gran molécula orgánica llamada grupo hemo y, de forma reversible, con una molécula de dioxígeno (O₂).
El color rojo intenso de la sangre se debe precisamente a este complejo de coordinación.
Otro ejemplo es la clorofila, el pigmento que permite a las plantas realizar la fotosíntesis, que es un complejo de coordinación con un ion de magnesio (Mg²⁺) en su centro.
En el ámbito industrial y cotidiano, los compuestos de coordinación también están muy presentes. El azul de Prusia, uno de los primeros pigmentos sintéticos, es un complejo de hierro.
Muchos catalizadores utilizados en la industria química para acelerar las reacciones son compuestos de coordinación de metales como el platino o el rodio.
Incluso en el tratamiento de aguas, se utilizan compuestos como el sulfato de alúmina para formar complejos que ayudan a precipitar las impurezas.
Su estructura única les confiere propiedades magnéticas, catalíticas y de color muy específicas.
El Lenguaje de la Química: Fórmulas para Representar Compuestos
Para poder estudiar, nombrar y comprender la inmensa variedad de compuestos químicos, los científicos han desarrollado un lenguaje universal basado en fórmulas.
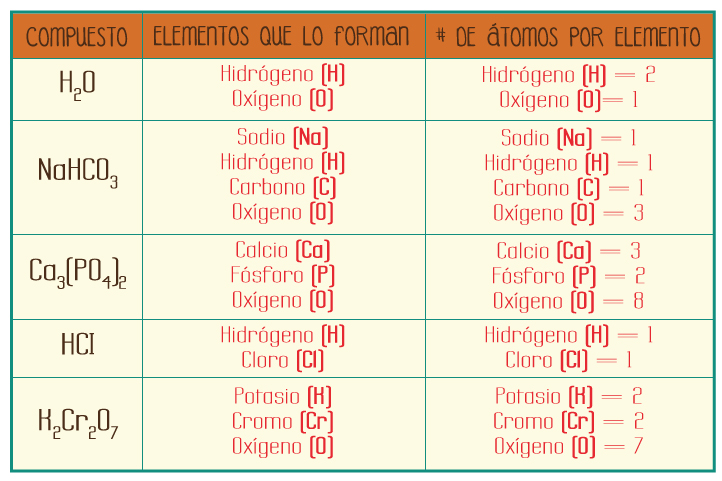
La representación más básica es la fórmula molecular (o fórmula química), que nos indica de manera concisa qué elementos forman el compuesto y cuántos átomos de cada uno hay en una sola molécula o unidad formular.
Se escribe utilizando los símbolos de los elementos seguidos de subíndices numéricos. Por ejemplo, la fórmula C₆H₁₂O₆ nos dice que una molécula de glucosa contiene 6 átomos de carbono, 12 de hidrógeno y 6 de oxígeno.
Sin embargo, la fórmula molecular a menudo no es suficiente, ya que diferentes compuestos pueden tener la misma fórmula molecular pero una estructura diferente; a estos se les llama isómeros.
Por ejemplo, tanto el etanol como el éter dimetílico tienen la fórmula C₂H₆O, pero sus propiedades son drásticamente distintas porque sus átomos están conectados de manera diferente.
Para resolver esta ambigüedad, se utiliza la fórmula desarrollada o estructural. Esta fórmula va un paso más allá y muestra gráficamente cómo están dispuestos los átomos y qué enlaces los unen entre sí.
La fórmula desarrollada puede ser más o menos detallada, desde una simple representación de los enlaces hasta modelos tridimensionales que muestran la geometría espacial de la molécula.
Ofrece una visión completa de la arquitectura molecular, lo que es fundamental para predecir y explicar las propiedades y la reactividad de un compuesto.
Para moléculas complejas como el ácido úrico (C₅H₄N₄O₃) o la lactosa (C₁₂H₂₂O₁₁), la fórmula desarrollada es indispensable para entender su estructura y su función biológica.
Estas fórmulas son el plano que permite a los químicos construir, modificar y entender el mundo a nivel molecular.
Conclusión: Un Universo de Combinaciones
Los compuestos químicos son, en esencia, los ladrillos con los que está construido el universo material.
Desde la sal que sazona nuestra comida hasta el ADN que codifica nuestra existencia, todo está regido por los principios de la combinación química.
Hemos visto que un compuesto es mucho más que la suma de sus partes; es una nueva sustancia con una identidad propia, forjada a través de la formación de enlaces químicos que alteran fundamentalmente las propiedades de los elementos constituyentes.
La clasificación en orgánicos e inorgánicos nos ofrece un primer mapa para navegar este vasto territorio, mientras que la distinción entre compuestos iónicos, moleculares y de coordinación nos revela la diversidad de estrategias que tienen los átomos para unirse y alcanzar la estabilidad.
Cada tipo de enlace confiere al compuesto un conjunto particular de características, determinando si será un sólido cristalino, un gas volátil, un pigmento colorido o una molécula biológicamente activa.
Finalmente, las fórmulas químicas, desde la simple fórmula molecular hasta la detallada fórmula desarrollada, nos proporcionan el lenguaje para describir, comunicar y manipular estas estructuras con precisión.
Entender los compuestos químicos no es solo una tarea para los científicos en un laboratorio; es una herramienta para comprender mejor el mundo que nos rodea, la vida misma y el potencial infinito que reside en la combinación de los elementos.
Son la manifestación tangible de que, en la química como en la vida, la unión crea una fuerza y una diversidad extraordinarias.
Te puede interesar...